[問題]. 次の本文について下の各問いに答えなさい。答の数値は有効数字三桁とする。必要あれば次の原子量を用いなさい。H=1.00, C=12.0, N=14.0, O=16.0
熱量計は, 注目物質のもつ熱量または反応により発生した熱量, いわゆる, 比熱, 潜熱, 反応熱などの熱量を測定する装置で, 熱量に対応する物理量の測定原理によって次のように大きく3つに分類される。
(1) 熱容量既知物質との混合状態でその温度変化を測定する。
(2) 二層平衡の潜熱既知物質の熱量吸収でその相変化を測定する。
(3) 一定量の電気エネルギー付加で注目物質の温度変化または相変化を測定する。
さらに(1)~(3)を改良したものがある。
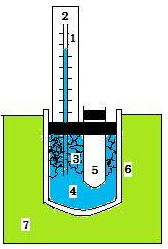
上の方法の中で, (2)に属する簡便型の氷熱量計の1例をあげると次図のようになる。ここで, 1:目盛, 2:ガラス細管, 3:氷, 4:水 5:反応容器, 6:デュワー瓶, 7:断熱シールド
反応容器内(5)で熱の出入りによる変化が生じると, 氷(3)の融解や水(4)の凝固が起こり, 同時にその体積変化がガラス細管(2)内の水のメニスカスの読み(1)として測定される。このことより, 水の融解と凝固に伴う体積変化は一対一に対応しているため、測定の難しい熱量を測定し易い「長さ」にして決めることが特長である。また, 氷と水が共存しているときは, デュワー瓶(6)内の温度を一定(0℃)に保持できる。
 (image156)
(image156)問1. 反応容器(5)内で 1.00mol/L(㍑)の6.00ml 塩酸と1.00mol/Lの6.00ml 水酸化カリウム水溶液を混合すると, メニスカスが9.05cm 下降した。この変化の熱化学方程式を書きなさい。
ただし, 反応熱はkJ単位, 氷の融解熱:6.00kJ/mol, 0℃での水と氷の密度:1.00g/cm3と0.917g/cm3, デュワー瓶内の水(4)と氷(3)の質量は90.0gと10.0g, ガラス細管の穴の断面積:0.0100cm2, 反応前の全反応物の温度:0℃とする。
答
問2. 反応容器(5)内で水10.0 ml に硝酸アンモニウム0.500gを溶かすと, メニスカスが4.40cm 上昇した。この変化の熱化学方程式を書きなさい。
答
問3. 反応容器(5)内で 6.00mol/Lの15.0ml 塩酸と6.00mol/Lの15.0ml 水酸化カリウム水溶液を混合すると, 氷がすべて溶けた。反応後の水の温度を求めなさい。水および溶液の比熱は一定で4.20J/(g・K)とし, デュワー瓶と反応容器の比熱は無視する。また, 反応前後の溶液の密度は1.00g/cm3とする。
答
問4. 問2でできた溶液を取り出し攪拌しながら徐々に冷却すると-2.3℃で凝固した。水のモル凝固点降下Kf [K・kg/mol]を希薄溶液の凝固点降下の式を使って求めなさい。
答
問5. 普通, 固体は融解すると体積が増加するが, 氷は減少する。この理由を分子間の結合の観点から100字以内で説明しなさい。
答