問1の答
 (image294)
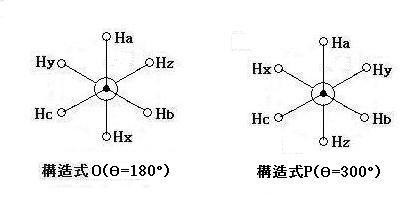
(image294)●図2から, 投影式OとPにおいて, θ= 180°と 300°では, エタン分子の回転エネルギーが共に低状態であるので, 図1の投影式Nと同じ形の投影式になる。ただし, 水素原子 Hx, Hy, Hz の位置が異なることになる。
θ= 180°… 180/360 = 1/2回転 : 図1の投影式M(θ= 0°)を基点にして時計方向に1/2回転する。
θ= 300°… 300/360 = 5/6回転 : 図1の投影式M(θ= 0°)を基点にして時計方向に5/6回転する。
問2の答
 (image296)
(image296)●図3から, 投影式Qでは,
θ= 0°… 0回転 : ブタン分子の回転エネルギーが極大値の最高状態であるので, このブタン分子の回転構造が最も不安定状態である。この不安定状態の主原因は, 体積がH原子に比べて大きな2つのCH3基が最接近した回転構造のために反発力が生じたことによる。
投影式Rでは,
θ= 60°… 60/360 = 1/6回転 : ブタン分子の回転エネルギーが極小値の準低状態であるので, このブタン分子の回転構造が準安定状態である。この準安定状態の主原因は, 体積がH原子に比べて大きな2つのCH3基が離れた回転構造のために反発力が弱まったことによる。1/6〜1/3回転では, CH3基と水素原子との反発力が生じて回転構造のエネルギーが高くなってくる。
投影式Sでは,
θ= 180°… 180/360 = 1/2回転 : ブタン分子の回転エネルギーが極小値の最低状態であるので, このブタン分子の回転構造が最も安定状態である。この安定状態の主原因は, 体積がH原子に比べて大きな2つのCH3基が最も離れた回転構造のために反発力が最小になったことによる。
問3の答
N, Pに対応する構造は2つの-COOHの距離が近いので水素結合を生じ安定する。
コハク酸(1,2-エタンジカルボン酸)の示性式は次のようになる。
HOOC-CH2-CH2-COOH
投影式 N, O に対応するコハク酸の構造式は下図のようになる。この図から, 投影式N(θ=60°)に対応する構造式は, 2つのカルボキシル基 -COOH が距離的に近いために, 分子中の1つのカルボキシル基の中にあるカルボニル基 -CO- が, もう1つのカルボキシル基中のヒドロキシル基 -OH と水素結合を生じる。したがって, この構造は安定化する。投影式P(θ=300°)に対応する構造式においても水素結合が生じるので安定化する。
投影式O(θ=180°)に対応する構造式では, 図に示しているように, 2つのカルボキシル基が離れているために水素結合が生じない。
したがって, 図1のHa, Hxの位置にそれぞれカルボキシル基を配置したコハク酸の場合, 投影式Oに対応する構造に比べて, 投影式Nおよび投影式Pに対応する構造がより安定することになる。
 (image297)
(image297)