[問題]. 周期表17族のフッ素, 塩素, 臭素, ヨウ素に関する次の各問いに答えなさい。
問1. 17族は別名何と言いますか。また, 何価の陰陽どちらのイオンになりやすいですか。
答
問2. 酸化力の順序はどのようになりますか。 答
問3. 17族の基底状態の電子配置おいて次の(ア)~(エ)には数字を, (a)~(d)には元素名を書き入れなさい。
(1) フッ素の電子配置は最外殻では(ア)個であるが内殻は(a)と同じである。
(2) 塩素の電子配置は最外殻では(イ)個であるが内殻は(b)と同じである。
(3) 臭素の電子配置は最外殻では(ウ)個であるが内殻は(c)と同じである。
(4) ヨウ素の電子配置は最外殻では(エ)個であるが内殻は(d)と同じである。
答
問4. 次の(1)~(4)の常温・常圧での状態に適合する17族の単体名を書き入れなさい。
(1) 赤褐色の液体である。 (2) 黄緑色の気体である。 (3) 黒紫色の固体である。(4) 淡黄色の気体である。
答
問5. 次の(1)~(4)の製法に関連する17族の単体名を書き入れなさい。
(1) 海水などに含まれる17族の成分をマグネシウム塩にしてその塩を硫酸酸性の酸化マンガン(IV)で酸化する。
(2) ホタル石や氷晶石に含まれる17族の成分をカリウム塩として溶融し電気分解する。
(3) 海草などに含まれる17族の成分をカリウム塩にしてその塩を硫酸酸性の酸化マンガン(IV)で酸化する。
(4) 海水や岩塩から得られる塩を溶融して電気分解する。
答
問6. 次の(1)~(7)の化学変化に関連する17族の単体名を書き入れなさい。また, その反応式を書きなさい。
(1) 臭化カリウム水溶液に加えると臭素が生成される。
(2) 水に常温で少量溶けかなりゆっくりと加水分解する。硝酸銀水溶液を加えると淡黄色沈澱を生じる。
(3) さらし粉または過マンガン酸カリウムに塩酸を加えると気体が発生する。
(4) 水と常温で激しく反応してガスを発生する。生成した水素化物はガラスを溶かす性質がある。硝酸銀水溶液を加えても沈澱を生じない。
(5) 酸化マンガン(IV)に塩酸を加え加熱すると気体が発生する。
(6) 水に常温でわずかに溶け加水分解はきわめて遅い。硝酸銀水溶液を加えると黄色沈澱を生じる。
(7) 水と常温で穏やかに反応して水素化物を生成する。硝酸銀水溶液を加えると白色沈澱を生じる。
答
問7. 酸化力(殺菌力)のあるヨウ素を含むうがい薬は溶媒として主に水が使われている。本来, ヨウ素は水にはほとんど溶けないがポリビニルピロリドンやヨウ化カリウムなどを水に入れると溶解度が上昇する。
水に対するヨウ化カリウム添加による溶解度上昇の原因は ヨウ化カリウムから生じるヨウ化物イオンで次のように三ヨウ化物イオンが形成されることによる。
I2 + I- ⇄ I3- … ①
①式の平衡定数Kは次式で表わされる。
K = [I3-]/{[I2][I-]} … ②
ただし, [I3-], {[I2]および[I-]はモル濃度を意味する。平衡定数Kは温度が一定であれば一定値を示す。いまの場合, Kは8.0×102 (mol/L)-1とする。
ヨウ素は四塩化炭素のような無極性の有機溶媒にはよく溶ける。このことより水に含まれるヨウ素を分液漏斗を使って抽出することができる。ヨウ素水溶液と四塩化炭素を分液漏斗に入れよく攪拌した後, 静置すると, ヨウ素は四塩化炭素の方へ移動する。この四塩化炭素溶液を取り出し溶媒の四塩化炭素(沸点:76.8℃)を蒸発させると後に固体のヨウ素が残る(抽出)。
分液漏斗中の混じり合わない四塩化炭素と水の二層では, ヨウ素は分配の平衡状態にあり, 四塩化炭素中のヨウ素モル濃度を[I2]t, 水中のヨウ素モル濃度を[I2]wとすると次の式が成立する。
KD = [I2]t/[I2]w … ③
KDは分配係数と言われ, 温度が一定であれば一定値を示す。いまの場合, KDは89.0とする。
次の(1)~(3)に答えなさい。答の数値は有効数字三桁とする。
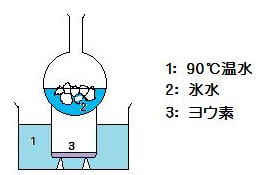
(1) 次図(image162)のように, ビーカーに少量のヨウ素を入れ, 上に氷水の入った丸底フラスコを乗せた。つぎにビーカーを90℃の温水で加熱した。ヨウ素はどのような変化が見られますか。図にならって結果を図示するとともに60字以内で簡潔に説明しなさい。
答
(2) 1.00L(㍑)の平衡状態のヨウ素-ヨウ化カリウム水溶液で, ヨウ素濃度は1.30×10-3mol/L, ヨウ化物イオン濃度は0.100mol/Lであった。加えたヨウ素の物質量はいくらですか。ただし, 水溶液中では上の①式以外の反応は起こらないものとする。
答
(3) 分液漏斗中で0.100mol/L ヨウ素の四塩化炭素溶液100mlにヨウ化カリウムを含む水溶液1.10L加えて十分攪拌した後, 分液漏斗を静置した。分配平衡状態に達したとき水層中のヨウ化物イオンの濃度は0.120mol/Lであった。分配平衡状態での水層中および四塩化炭素層中のヨウ素の物質量はいくらですか。ただし, 四塩化炭素中にはI2のみが存在し, 平衡状態の水溶液中では上の①式以外の反応は起こらないものとする。
答