問1の答 m = 3, n = 2
本文図1の正四面体SiO4での酸素共有構造において, 鎖状イオン骨格を次のように書き直すことができる。
……-SiO3-SiO3-SiO3-……
この骨格部分の最小単位のSiO3において, Si原子中の最外殻電子は4個の sp3 混成軌道を形成している。
そこへ3個の酸素原子が, それぞれ自分自身の1個の最外殻不対電子 2p を使って, 対になって共有結合する。 このとき, 1個の酸素原子は, もうひとつ存在する 1個の最外殻不対電子 2p を使って, 隣りのSi原子中の4個のsp3 混成軌道の内の1個と対になって共有結合する。
他の2個の酸素原子の最外殻不対電子 2p は, 外部から2個電子を受け取って, 対となり安定化する, いうゆる, 2価の負電荷を帯びる。
また, 残りの Si原子中の sp3 混成軌道 1個は隣りの酸素原子の最外殻不対電子 2p と対になり共有結合する。
以上より,
……-(SiO32-)-(SiO32-)-(SiO32-)-……
問2の答 石英または水晶
石英の組成式はSiO2であるが, それは次のようにして決められる。
本文図1の正四面体SiO4で全て酸素を共有した構造は次のように書き直すことができる。
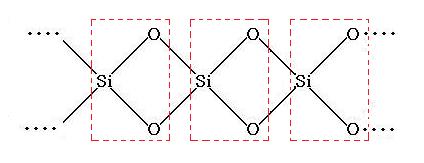 (image315)
(image315)上図の分子式は, n を正の整数とすると,
(SiO2)n
組成式は,
SiO2
問3の答 a = -3b - 4c + 2d, d = 2(b + c)
○原子はプラスになり易い陽性元素とマイナスになり易い陰性元素に大きく2つに分けられる。これを数値化したものが酸化数である。化合物中では, 基準として, 普通, 水素原子は+1, 酸素原子は-2である。また, 電気的に中性の化合物では, その原子の酸化数の総和はゼロで, 複数の原子からなるイオンでは, その原子の酸化数の総和はイオンの価数に等しい。
○ SiO2のSi の酸化数を x , Al2O3のAl の酸化数を y とすれば,
x + (-2)×2 = 0 よって, x = +4 …Si の酸化数
2y + (-2)×3 = 0 よって, y = +3 …Al の酸化数
○ 問題本文中にあるゼオライトとしてのアルミノケイ酸塩の一般式は
MaAlbSicOd・eH2O
ここで, 酸化数において, 結晶中の水分子のeはa,b,c,d とは直接関係ない。そこで, MaAlbSicOd の各原子の酸化数において次式が成立する。ただし, MはNa, K, Caなどの陽イオンになり易い金属なので, その酸化数は+1である。
(+1)×a + (+3)×b + (+4)×c + (-2)×d = 0
よって,
a = -3b - 4c + 2d
○ 問題本文中の図2のネットワーク構造を参照すると, SiO2が m個のAlO2-に置き換わると,
(SiO2)n - m(AlO2-)m = [Sin - mAlmO2n]m-
よって, Mの酸化数は +1 から
MmAlmSin - mO2n
問題本文中にあるゼオライトとしてのアルミノケイ酸塩の一般式 MaAlbSicOd・eH2O を比べると,
a = b = m
c = n - m
d = 2n
よって,
d = 2n = 2(m + c) = 2(b + c)
問4の答
AlO2-が(SiO2)nでSiO2の半分以上置換すると隣接正四面体間に負電荷の反発が起る。
問5の答
12Na2SiO3・9H2O + 12NaAlO2 → Na12Al12Si12O48・27H2O + 24NaOH + 69H2O
x mol のケイ酸ナトリウム Na2SiO3・9H2O と y mol のアルミン酸ナトリウム NaAlO2 が反応して z mol のA型ゼオライトNa12Al12Si12O48・27H2O が生じたとする。その他の生成物にはAlやSiを含むものはないと考えられる。そこで,
xNa2SiO3・9H2O + yNaAlO2 → zNa12Al12Si12O48・27H2O + pNaOH + qH2O
上式において次式が成立する。
Naにおいて,
2x + y = 12z + p …①
Siにおいて,
x = 12z …②
Oにおいて,
12x + 2y = 75z + p + q …③
Hにおいて,
18x = 54z + p + 2q …④
Alにおいて,
y = 12z …⑤
よって, ②と⑤を①に代入すると,
2(12z) + (12z) = 12z + p, p = 24z …⑥
②,⑤,⑥を③に代入すると,
12(12z) + 2(12z) = 75z + (24z) + q, q = 69z …⑦
ここで, z = 1 とすると, ②,⑤,⑥,⑦において,
x = 12, y = 12, p = 24, q = 69
以上より,
12Na2SiO3・9H2O + 12NaAlO2 → Na12Al12Si12O48・27H2O + 24NaOH + 69H2O
○ アルミニウムやケイ素などを含む化合物は, 強アルカリ水溶液中ではゲル状化合物を生成する。例えば, 水酸化ナトリウム水溶液中では, 酸化アルミニウムAl2O3はゲル状のテトロヒドロキソアルミン酸ナトリウムNa[Al(OH)4]を生じる。
Ai2O3 + 2NaOH + 3H2O → 2Na[Al(OH)4]
また, 水溶液中のテトロヒドロキソアルミン酸イオンとアルミン酸イオンは, 水温に対応して, 次のように可逆的に変化する。
[Al(OH)4]- ⇄ AlO2- + 2H2O
問6の答 1.1×102 [mg]
A型ゼオライトNa12Al12Si12O48・27H2O がカルシウムイオンCa2+と交換反応すると,
Na12Al12Si12O48・27H2O + 6Ca2+ → Ca6Al12Si12O48・27H2O + 12Na+ …①
そこで, A型ゼオライトの式量 N は,
N = 23×12 + 27×12 + 28.1×12 + 16×48 + 18×27 = 2191.2
1.0 g のA型ゼオライトの物質量 M [mol] は, 式量Nを用いて,
M = 1.0/N = 1.0/2191.2 = 4.564×10-4 [mol]
カルシウムイオンCa2+の質量 W は, カルシウムの原子量 40.1を用いて,
W = 40.1×(4.564×10-4)×6 = 0.1098 [g] = 10.98 [mg] ≒1.1×102 [mg]
問7の答
石けんの洗浄作用の保持のため洗濯液を常に硬水から軟水にする。
石けん(高級脂肪酸のNa塩:RCOONa)にCa2+やMg2+などを含む硬水を使用すると, 次の反応式のように, 難溶のCa塩:Ca(RCOO)2などが沈殿して水溶液中の石けんの洗浄作用を無能にする。
2RCOONa + Ca2+ → Ca(RCOO)2↓ + 2Na+