[問題] 次文はマイケル・ファラデーによる1860年のクリスマス・レクチャー「ロウソクの化学」の抜粋である。これを読み, 後の II の問題に答えなさい。
「レクチャー 1- ロウソク:炎とその源・形・動き・光」より
私達は, 皆さんがこうして, ここでの催しに関心を持たれて, 見に来て下さったことを光栄に思います。そのお礼に, このレクチャーで「ロウソクの化学」をご覧に入れようと思っています。
…(中略)…
気流の向き次第で, 炎は上にも下にも向くことをお目にかけましょう。この小さな実験装置で簡単にできます。今度はロウソクではありません。煙が少ないアルコールの炎を使います。
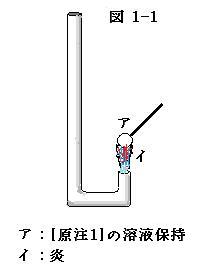
ただ, アルコールだけの炎は見にくいので, 別の物質[原注1]で炎に色をつけています。炎を下に吹いてやると, 気流が曲がるように細工した, この小さな煙突に, 炎が下向きに吸い込まれていくことがわかるでしょう(図1-1)。
[原注1]:アルコールに塩化銅(II)を溶かしてあった。
 (image430)
(image430)「レクチャー 2〜3 - 炎の出す光・水の生成・他」より
…(中略)…
この黒い物質は何でしょうか?それはロウソクの中にあるのと同じ炭素です。それは明らかにロウソク中に存在していたはずです。そうでなければここにあるはずがありません。固体の状態を保っている物質は, それ自身が燃えるものであろうが, なかろうが, 炎の中で明るく輝くのです。
これは白金製の針金です。高温でも変化しない物質です。これを炎の中で熱してみると明るく輝いているのがわかるでしょう。炎自身の光が邪魔にならないように, 炎を弱くしてみます。それでも炎が白金に与えられている熱は―炎自身の熱よりずっと少ないのですが―白金を輝かせています。
…(中略)…
ここにはまた(別のビンを取りながら), オイルランプの燃焼で作られた水があります。1リットル(訳注1)の油をきちんと完全に燃やすと, 1リットル以上の水が生成します。こちらは蜜ロウソクから長い時間をかけて作った水です。このように, ほとんどの燃える物質は, ロウソクのように炎を出して燃える場合, 水を生成することがわかります。
「レクチャー 4 - ロウソクの中の水素・燃えて水に・水の他の成分・酸素」 (略)
「レクチャー 5 - 空気中の酸素・大気の性質・二酸化炭素」より
…(中略)…
この物質をたくさん手に入れる, いい方法があります。おかげで, この物質のいろいろな性質を探求することができます。この物質は, ほとんどの皆さんが予想もしない所に大量にあります。
石灰石はどれでも, ロウソクから発生するこの気体―「二酸化炭素」と言います―を大量に含んでいます。チョーク(訳注2)も貝殻もサンゴも皆, この不思議な気体をたくさん含んでいます。この気体はこういう石の中に「固定」されているのです。
そして, これはとても重い気体です。空気よりも重いのです。その質量を, 表1-1の中の一番右に書いておきました。私達がこれまでに見てきた他の気体の質量も, 比較のために示してあります。
表1-1 標準状態(0℃, 1atm)における28.0Lの気体の質量(訳注1)
水素 2.50g 酸素 40.0g 窒素 35.0g 空気 36.0g 二酸化炭素 57.0g
「レクチャー 6 - 炭素/炭・石炭ガス・呼吸―燃焼との類似性・結び」より
ご覧に入れたように, 炭素は固体の形のままで燃えます。そして皆さんがお気付きのように, 燃えた後は固体ではなくなるのです。このような燃え方をする燃料は, あまり多くはありません。
…(中略)…
ここにもう一つ, よく燃える, 一種の燃料があります。Eご覧のように空気中に振りまくだけで発火します。(発火性鉛[原注2]の詰まった管を割りつつ)この物質は鉛です。とても細かい粒子になっていて, 空気が表面にも中にも入り込めるので燃えるのです。
しかし, こうやって(管の中身を, 鉄板の上に山のように積み上げる), かたまりにすると燃えないのはどうしてでしょうか?そう, 空気が入って行けないのです。まだ下に燃えていない部分があるのに,生成したものが離れてくれないので, 空気に触れることができず, 使われずに終わってしまうのです。
何と, 炭素と違うことでしょう!F先ほどご覧に入れたように, 炭素は燃えて, 灰を残さずに酸素の中に溶け込んでいきます。ところが, ここには(燃えた発火性鉛の灰を指して)燃やした燃料よりも沢山の灰があります。酸素が一体化した分だけ, 重たいのです。これで皆さんは, 炭素と鉛や鉄の違いがお分かり頂けたことと思います。
[原注2]:発火性鉛は乾燥した酒石酸鉛をガラス管(片方を封じ, 他方を絞っておく)中で, 気体の発生がなくなるまで加熱することで得られる。最後にガラス管の開いてあった端をバーナの火で封じる。管を割って中身を空中に振り出すと, 赤い閃光を出して燃える。
(Michael Faraday, "The Chemical History of a Candle", Dover, New York, 2002より)
(訳注1):原文のヤード・ポンド法による記述は, 意図を損なわぬよう書き改めた。
(訳注2):日本では, これと異なる物質でできたチョークも多く使われている。
II. 鉛の燃焼直後の状態を考察するために, 以下の問1と2に答えなさい。必要であれば次の数量を用いなさい。原子量 H=1.00, C=12.0, N=14.0, O=16.0, Ca=40.1, Pb=207.2, 生成熱(25℃)[単位:kJ/mol] CO2(気):394, PbO(固):219, PbO2(固):274
[問題]の文において, ファラデーは下線部EとFのように炭素と鉛の燃え方の違いを述べている。炭素が燃焼するときには, 二酸化炭素が散逸するのに対して, 鉛が燃焼するときには, 酸化生成物が散逸せずに留まっている。
問1. 燃焼直後の高温状態では, 鉛の酸化物中で一酸化鉛(PbO)が最も安定である。鉛が燃焼して, 固体の一酸化鉛を生成する反応の熱化学方程式を書きなさい。
答
問2. 燃焼する前の鉛と酸素の温度は25℃であるとし, 燃焼反応の反応熱は全て生成物の温度上昇と融解と蒸発に使われるものとする。このとき, 燃焼直後の生成物の状態は, 固体, 液体, 気体の何れであるかを, あるいはこれらの共存状態であるかを記し, その温度を求めなさい。
生成物が共存状態である場合は, それぞれの物質量の比も記すこと。また, 答に至る計算過程も示しその答の数値は有効数字二桁とする。
物質1molの温度を 1K上げるために必要な熱量を「モル比熱」と呼び, 一般に温度の関数である。ただし, 生成物である一酸化鉛については, 固体, 液体, 気体の各状態の範囲内で, ほぼ一定とみなすことができる。その値を, 融点, 融解熱, 沸点, 蒸発熱とともに, 以下に示す。
モル比熱[単位:JK-1・mol-1] PbO(固):55, PbO(液):65, PbO(気):38, PbO(固)融点:885℃, 融点における融解熱:26[kJ/mol], PbO(液)沸点:1725℃, 沸点における蒸発熱:223[kJ/mol]
答