問1の答 下図1参照
(実験1)から, 化合物 H の分子式は, 炭素数 3 で分子量 42 であるので, C3Hn とすることができるので, その分子式から次式が成立する。
12×3 + 1×n = 42
n = 6
よって, H の分子式は
C3H6
H は付加の重合反応で, 熱可塑性を持つポリマー X を得るので
… + CH(CH3)=CH2 + CH(CH3)=CH2 + … → … -CH(CH3)-CH-CH(CH3)-CH- …
上式を書き直すと,
nCH(CH3)=CH2 → [-CH(CH3)-CH-]n
以上から, H と X の示性式は
H(プロペン) : CH(CH3)=CH2
X(ポリプロピレン) : [-CH(CH3)-CH-]n
一方で, 化合物 H を触媒存在下で酸素によって酸化すると,
CH(CH3)=CH2 → (触媒下で酸化) → CH2=CH-CO-OH (分子量 72)
そこで, I は
I (アクリル酸): CH2=CH-CO-OH (沸点 141℃)
I と炭酸水素ナトリウムとの反応では,
CH2=CH-CO-OH + NaHCO3 → CH2=CH-CO-ONa + H2O + CO2
よって, 塩 J は
J (アクリル酸ナトリウム): CH2=CH-CO-ONa
I とメタノールとの反応では, 水が生じるので (エステル化)
CH2=CH-CO-OH + CH3OH → CH2=CH-CO-OCH3 + H2O
よって, K (エステル)は
K(アクリル酸メチル) : CH2=CH-CO-OCH3 (沸点 80℃)
上述のように, 二重結合を持つ H, I, J, K は臭素と次のように付加反応する。
CH(CH3)=CH2 + Br2 → CH(CH3)Br-CH2Br
CH2=CH-CO-OH + Br2 → CH2Br-CHBr-CO-OH
CH2=CH-CO-ONa + Br2 → CH2Br-CHBr-CO-ONa
CH2=CH-CO-OCH3 + Br2 → CH2Br-CHBr-CO-OCH3
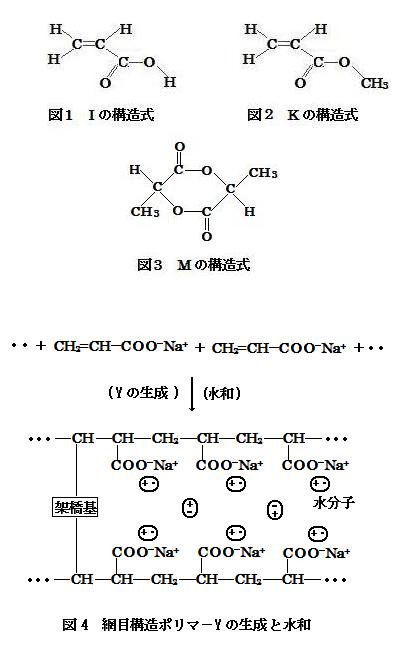
I と K の構造式は, 構造式の例を参照して, 下図( )のようになる。
問2の答
[構造式] 下図2参照
[説明] Iには水素結合が存在するためその沸点が大きい。
物質の沸点は, 理論的に, 所定の圧力の飽和蒸気圧とその液体とが平衡に共存し得る温度である。このとき, 液体の物質は, その粒子の蒸発が物質粒子間の相互作用を断ち切って液面ばかりでなく液体の内部からも生じ沸騰する(一般に所定の圧力は 1 atm)。そこで, 沸点は主としてその液体物質の粒子間の相互作用による結合の強弱に依存する。
K と I の示性式は, 問1の解説を参照して
K : CH2=CH-CO-OCH3 (沸点 80℃, 分子量86)
I : CH2=CH-CO-OH (沸点 141℃, 分子量72)
上述の示性式において, K の分子はエステル結合を有し, ほぼ無極性分子として挙動する。ゆえに, K の分子間の相互作用は, ファンデルワールス力だけに関連している。したがって, H の沸点は, 主として, その 分子間のファンデルワールス力での弱い結合に依存する。
一方, I はカルボン酸に属しその分子中にカルボキシル基を有している。そのために, I の分子間に水素結合が存在する。ゆえに, I の分子間の相互作用は, ファンデルワールス力に加えて水素結合によるものが関連している。したがって, I の沸点は, ファンデルワールス力での結合と共に, より強い水素結合に依存するので, 大きくなる。ここで, K と I のファンデルワールス力は, 分子量 86 と 72 を考慮すると, あまり違わない。
問3の答 (2)
問1の解説を参照して, J (CH2=CH-CO-ONa)に架橋剤を加えて重合を行うと, 網目構造をもつポリマー Y が, 下図4の反応のようにして得られる。Y の網目構造の空隙は, 下図4から分かるように, -COO-Na+ が多く存在している。そのために Y は極性分子の水分子と水和し多くの水を取り込んで保持し膨潤する。
問4の答
Y分子の内外の溶液濃度差で水和分子が外へ浸透する。
Y の網目構造表面の半透膜作用で, 網目構造の内部と外部の炭酸カルシウムの濃度差により, 網目構造内の水和していた水分子が外部へ浸透する。
問5の答 下図3参照
酵素によるグルコース C6H12O6 の分解反応で
C6H12O6 →(分解)→ 2C3H6O3
化合物 L(C3H6O3)が得られる。その L は炭酸水素ナトリウムと反応して水溶性の塩を生じることからカルボン酸であることが想定される。また, 不斉炭素を有している。そこで, L の示性式は次のようになる。C* は不斉炭素を表わしている。
HOC*H(CH3)COOH (乳酸)
上述の L を脱水縮合すると
2HOCH(CH3)COOH → (*-OCH(CH3)COOCH(CH3)CO-*) + 2H2O
化合物 M:(*-OCH(CH3)COOCH(CH3)CO-*) が得られる。ただし, 左端と右端の*は互いに結合していることを表わしている。分子式は C6H8O4 である。
化合物 M を重合するとポリ乳酸のポリマー Z:(-OCH(CH3)COOCH(CH3)CO-)n が得られる。
n(*-OCH(CH3)COOCH(CH3)CO-*) → (-OCH(CH3)COOCH(CH3)CO-)n
M の構造式は, 構造式の例を参照して, 下図( )のようになる。
問6の答 (3)
ポリマーZの分子内にエステル結合を有している。したがって, 土壌中に触媒作用をする物質がわずかに存在すると, エステル結合は次のように容易に加水分解して乳酸などの低分子量化合物に変換される。
(-OCH(CH3)COOCH(CH3)CO-)n + 2nH2O → 2nHOCH(CH3)COOH
 (image513)
(image513)