問1の答 (エ)
(b)において,
(i) 図1を参照して, ペプチドグリカンを構成する多糖(…-S1-S2-…)は, N-アセチルグルコサミン(S1) と N-アセチルムラミン酸(S2) が, 交互に β-1,4-グルコシド結合したものである。
(ii) N-アセチルグルコサミンは, グルコースの2位の炭素原子に結合したヒドロキシ基がアミノ基に置換され, さらにそのアミノ基がアセチル化された化合物である(図2参照)。
(iii) N-アセチルムラミン酸は, N-アセチルグルコサミンの3位の炭素原子に結合したヒドロキシ基にエーテル結合した化合物である(図2参照)。
上の(i), (ii) (iii), および下の●2を考慮すると,
図2の(ア)はα-1,4-グルコシド結合および R1 はエステル結合で不適合, 図2の(イ)はβ-1,4-結合および R2 はエステル結合で不適合, 図2の(ウ)はα-1,4-グルコシド結合および R3 はエーテル結合で不適合, 図2の(エ)はβ-1,4-結合および R4 はエーテル結合で適合する。
[学習]
●1 天然高分子には, 単量体のグルコース, アミノ酸, イソプレンが多数結合した多糖類, タンパク質, 天然ゴムなどがある。その他にも自然界には天然高分子が多数存在している。
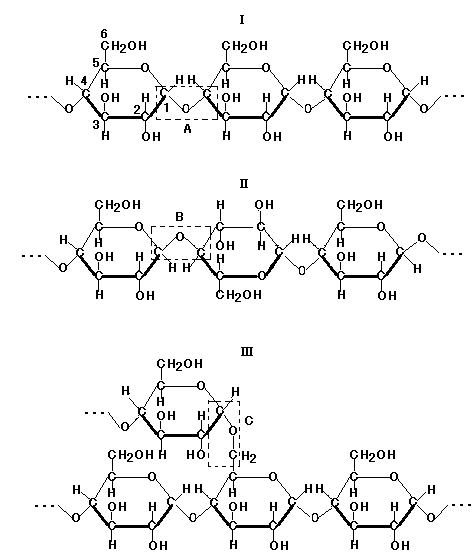
●2 下図(image145)の構造は, I:アミロース(α-グルコースが直鎖状に結合。A:点線四角内はα-1,4-グリコシド結合部を表す), II:セルロース(β-グルコースが直鎖状に結合。B:点線四角内はβ-1,4-グリコシド結合部を表す), III:アミロペクチンとグリコーゲン(α-グルコースが直鎖状に結合し, さらにα-1,6-グリコシド結合により枝分かれする。C:点線四角内はα-1,6-グリコシド結合部を表す)…動物の肝臓や筋肉に蓄えられるグリコーゲンはアミロペクチンよりも枝分かれが多い。
●3 デンプンは希硫酸溶液中で長時間放置しておくと完全に加水分解して単糖類のグルコースになる。平衡状態では次の図(image146)のように3種のα-グルコース…IV, アルデヒド型グルコース…V, β-グルコース…VIが存在する。アルデヒド型グルコースには分子中にアルデヒド基が存在し還元性を示す。

●4 [平均分子量]…高分子の分子量は単一ではなく種々の分子量をもつ分子の混合物である。どんなに分別しても単一分子量の試料を得ることはできない。したがって, 高分子には分子量分布曲線が存在する。
高分子の分子量は平均分子量が用いられる。ふつう高分子の分子量は次式の数平均分子量を意味する:
高分子の数平均分子量 = (ΣMiNi)/(ΣNi) ただし, Mi:i分子の分子量, Ni:i分子の数
数平均分子量以外に, 重量平均分子量, Z平均分子量(超遠心機使用), 粘度平均分子量などがある。
問2の答
A1とA4 : アラニン A2 : グルタミン酸 A3 : リシン A5 : グリシン
(1) ペプチドグリカン → (加水分解) → アミノ酸 A1, A2, A3, A4, A5
(2) A1 は A4 の光学異性体であり, A5 には光学異性体が存在しない。
(3) 下図3を考慮すると, 5つの各アミノ酸の示性式は次のようになる。
(i) グリシン NH2-CH2-COOH (ii) アラニン NH2-C*H(CH3)-COOH
(iii) グルタミン酸 NH2-C*H((CH2)2COOH)-COOH (iv) リシン NH2-C*H((CH2)4NH2)-COOH
ここで C* は不斉炭素原子(下の●5の3参照)を表わしている。(i)~(iv) のうちで (i) のグルシンには不斉炭素原子がない。したってグリシンには光学異性体が存在しない。上の(2)において A5 には光学異性体が存在しないので
A5 : グリシン
(5) 各アミノ酸は水溶液中では次のような平衡状態となる。
(i) グリシン
NH3+-CH2-COO-(aq) ⇄ NH3+-CH(H)-COO-(aq)
(ii) アラニン
NH3+-CH(CH3)-COO-(aq) ⇄ NH3+-CH(CH3)-COO-(aq)
(iii) グルタミン酸
NH3+-CH((CH2)2COOH)-COO-(aq) ⇄ NH3+-CH((CH2)2COO-)-COO-(aq) + H+(aq)
(iv) リシン
NH3+-CH((CH2)4NH2)-COO-(aq) + H2O ⇄ NH3+-CH((CH2)4NH3+)-COOH(aq) + OH-(aq)
上の(2), 上の表1および下の●6から,
○1 (ii)のアラニンの平衡状態を考慮すると, A1とA4は分子式は同じで光学異性体の関係にあるので, それらの等電点は同値(6.0)で中性の pH 7.0 に近いことが考えられる。したがって
A1とA4 : アラニン
ただし, pH が 7.0 でなく 6.0 の酸性側になっているのは, アラニン NH2-CH(CH3)-COOH において, 双生イオンを生成する時に
NH2-CH(CH3)-COOH(aq) ⇄ NH2-CH(CH3)-COO-(aq) + H+(aq) …(a)
NH2-CH(CH3)-COO-(aq) + H+(aq) ⇄ NH3+-CH(CH3)-COO-(aq) …(b)
上の平衡 (a), (b) での平衡定数の値に依存して H+ が多くなり, pH<7 となるためである。
○2 (iii)のグルタミン酸の平衡状態を考慮すると, 酸性の水溶液で平衡が左辺に移動して双生イオン NH3+-CH((CH2)2COOH)-COO- が生成される。そこで等電点は酸性側の 3.22 になると考えられる。したがって,
A2 : グルタミン酸
○3 (iv)のリシンの平衡状態を考慮すると, 塩基性の水溶液で平衡が左辺に移動して双生イオン NH3+-CH((CH2)4NH2)-COO- が生成される。そこで等電点は塩基性側の 9.74 になると考えられる。したがって,
A3 : リシン
[学習]
●5 有機化合物において, 分子式は同じでも構造が異なるために物理的・化学的性質が異なる物質が複数個生じる場合がある。この複数個の物質は互いに異性体の関係にあるという。その異性体の分類は, 1つの方法として, 次のように大きく分けて3つになる。
1. 構造異性体…1つの分子式で表される分子の原子間の結合を価標(結合線)で平面上に図式的に描くと, 異なった構造式が生じる場合に相当する。
2. 互変異性体…1つの分子式で表せる分子が炭素原子間に不飽和結合を有し分子中の少なくとも1個の原子の相対的位置が著しく違うと, 異なった構造式が生じる場合に相当する。
3.立体異性体(三次元の全原子間距離は異性体間で同じ)
○幾何異性体…有機化合物の炭素原子間の二重結合を挟んで結合する置換基の配置で, 異なった構造式のシスcisとトランスtransが生じる場合に相当する。
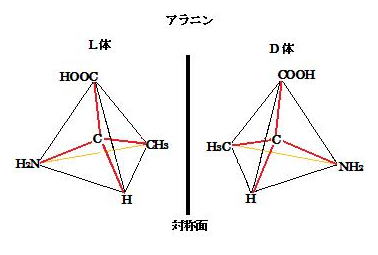
○光学異性体…分子に不斉炭素原子(4価の炭素原子に4個の異なる原子または原子団などが結合)があると、実像と鏡像の関係にある一対の対掌体(右手と左手の関係)の分子が存在する。この2種の分子に直線偏光が当ると、各々の分子において、その光の偏光面が右旋性の回転(+またはd)をするか左旋性の回転(-またはl:エル)をする…光学活性となる。この2つの分子は光学異性体の関係にあるという。
[例] アラニンの光学異性体
示性式 : H2N-C*H(CH3)-COOH (C*は不斉炭素原子を表す。この炭素原子に結合している原子または原子団は全て異なる…-NH2, -H, -CH3, -COOH)
L-アラニンおよび D-アラニンの 2つの光学異性体存在
図示すると下図のようになる。
 (image154)
(image154)○ その他(上の幾何と光学の異性体以外で回転や反転などによって生じる立体異性体)
●6 アミノ酸およびアミノ酸分子が2個以上アミド結合 (-NH-CO-) したペプチドにおいて,
その溶液は, pHに依存して電気二重層の電位が正または負となる。そして, この中間に電位がゼロになるpHが存在し, このpHが等電点である。等電点でのその分子は双生イオン(電気的に中性)と呼ばれている。
等電点では, その分子に含まれる塩基性解離基の数と酸性解離基の数が等しくなり, 実効荷電がゼロとなったときのpHである。そのとき, 分子内で正と負の電荷が打ち消され, 電気泳動が見られなくなる。
その分子中の塩基性解離基は, アミノ基-NH2, ヒスチジンの4-イミダゾリル基C3H3N2-, アルギニンのグアニジノ基NH2C(NH)NH-などである。一方, 酸性解離基は, カルボキシル基-COOH, チロシンのフェノール性水酸基-OH, シスチンのメルカプト基-SHなどである。
その分子の塩基性基に結合したプロトン数と酸性基から解離したプロトン数が等しくなったときのpHを特に等イオン点と呼んでいる。等イオン点は塩類などの添加で変化する。
●7 アミノ酸はα, β, γなどに分類される。その中でα‐アミノ酸の一般の分子式は R‐CH(NH2)COOH で表わされ, 同一炭素原子にアミノ基-NH2とカルボキシル基-COOHが結合する両性電解質である。実際の水溶液中では, 水素イオン濃度に応じて陽と陰のイオンおよび双生イオンの3つのイオンとして存在している。結晶は双生の特定の配列集合である。
グリシン以外のα‐アミノ酸は分子中に不斉炭素を含むので光学異性体が存在する。自然界はほとんどL体のα‐アミノ酸である。2個以上のアミノ酸は脱水によってアミド結合いわゆるペプチト結合:-NH-CO- をしてジ, トリ, …, ポリ, マクロなどのペプチドを生成する。
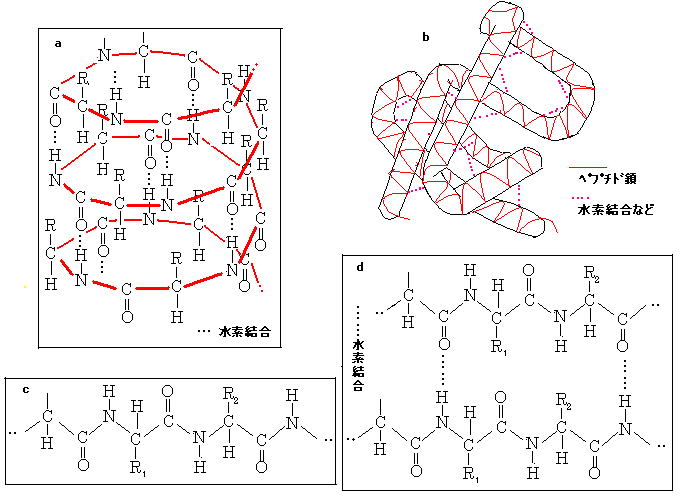
天然高分子のタンパク質は, 主にグリシン, アラニンなどの20種類のα‐アミノ酸から成り立つポリマーのペプチドで 1次構造のペプチド鎖を形成している。ペプチド鎖中にはカルボニル基-CO とイミノ基-NH が存在するので, それらは水素結合 して一定の 2次構造をとる。
ポリペプチド鎖内の水素結合によるらせん状のα形やポリペプチド鎖間の水素結合によるシート状のβ形は 2次構造に相当する。さらに, らせん状のα形は, それらの間で, 水素結合, アミノ酸残基によるイオン結合:-NH3+…COO‐-, およびジスルフィド結合:-S-S-で球状や繊維状などの 3次構造をとる。その他の高次構造も存在する。タンパク質の高次構造はその機能性と密接な関係にある。
例として生体触媒作用を示す酵素があげられる。α‐グルコシダーゼという酵素は, α‐D‐グルコシドだけに作用し, 立体異性体のβ‐D‐グルコシドには全く作用しないという特異性を示す。これは, 主として, 酵素の主成分であるタンパク質の構造が基質のα‐D‐グルコシドと立体的にマッチしているがβ‐D‐グルコシトとはマッチしていないことを意味する。同時に, 反応速度が活性化エネルギーの小さい径路で促進され, 化学変化がタンパク質に結合している原子団や分子団の作用基で生じる(下図参照 image102)。
問3の答 5種類
● ペプチドのアミド結合 -CO-NH- は, アミノ酸分子のカルボキシル基 -COOH と アミノ基 -NH2 が脱水反応をすることによって形成される。
(…-COOH) + (…NH2) → …CO-NH… + H2O
● A2のグルタミン酸分子 NH2-CH((CH2)2COOH)-COOH には,
カルボキシル基(記号:cr)…cr1, cr2
アミノ基(記号:am)… am1
● A3のリシン分子 NH2-CH((CH2)4NH2)-COOH には,
カルボキシル基(記号:cr')…cr'1
アミノ基(記号:am')… am'1, am'2
● そこで, A2のグルタミン酸とA3のリシンの脱水によるジペプチド形成において, アミノ基とカルボキシル基の組み合わせは次のように 5種類になる。
cr1-am'1, cr1- am'2, cr2-am'1, cr2-am'2, am1-cr'1
具体的に反応式で示すと, 次の(i)~(v)のようになる。
NH2-CH((CH2)2COOH)-COOH + NH2-CH((CH2)4NH2)-COOH →
NH2-CH((CH2)2COOH)-CO-NH-CH((CH2)4NH2)-COOH + H2O …(i)
NH2-CH((CH2)2COOH)-COOH + NH2-CH((CH2)4NH2)-COOH →
NH2-CH((CH2)2COOH)-CO-NH-(CH2)4-CH(NH2)-COOH + H2O …(ii)
NH2-CH((CH2)2COOH)-COOH + NH2-CH((CH2)4NH2)-COOH →
NH2-CH(COOH)-(CH2)2-CO-NH-CH((CH2)4NH2)-COOH + H2O …(iii)
NH2-CH((CH2)2COOH)-COOH + NH2-CH((CH2)4NH2)-COOH →
NH2-CH(COOH)-(CH2)2-CO-NH-(CH2)4-CH(NH2)-COOH + H2O …(iv)
NH2-CH((CH2)2COOH)-COOH + NH2-CH((CH2)4NH2)-COOH →
HOOC-CH((CH2)2COOH)-NH-CO-CH((CH2)4NH2)-NH2 + H2O …(v)
問4の答
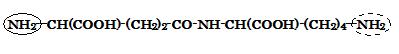 (image540)
(image540)●1 「ペプチドグリカン中の A2 と A3 の間, および A3 と A5 の間の結合は, 通常のペプチド結合ではなく, アミノ酸側鎖(R)に含まれる官能基が関与するアミド結合である。」こと, および図1と問4の解説を考慮すると,
…S1-S2(A1-A2-A3(A5-…)-A4…
●2 S2-A1 の結合は, S2の側鎖R4中の-COOH基とA1中の-NH2基の脱水反応によって, 形成される。
…-CO-NH-CH(CH3)-CO-OH
ここで, S2は N-アセチルムラミン酸, A1はアラニン NH2-CH(CH3)-COOH である。
●3 A1-A2 の結合は, A1中の-COOH基とA2中の-NH2基の脱水反応によって, 形成される。
NH2-CH(CH3)-CO-NH-CH((CH2)2COOH)-COOH
ここで, A2はグルタミン酸 NH2-CH((CH2)2COOH)-COOH である。
●4 A2-A3 の結合は, A2中の側鎖-COOH基とA3中の-NH2基の脱水反応によって, 形成される。
NH2-CH(COOH)-(CH2)2-CO-NH-CH((CH2)4NH2)-COOH
ここで, A3はリシン NH2-CH((CH2)4NH2)-COOH である。
●5 A3-A4 の結合は, A3中の-COOH基とA4中の-NH2基の脱水反応によって, 形成される。
NH-CH((CH2)4NH2)-CO-NH-CH(CH3)-COOH
ここで, A4はアラニン NH2-CH(CH3)-COOH である。
●6 A3-A5 の結合は, A3中の側鎖-NH2基とA5中の-COOH基の脱水反応によって, 形成される。
NH2-CH(COOH)-(CH2)4-NH-CO-CH2-NH2
ここで, A5はグリシン NH2-CH2-COOH である。
以上から, ジペプチド A2-A3 において, ●3, ●4, および●6 を考慮すると,
NH2-CH(COOH)-(CH2)2-CO-NH-CH(COOH)-(CH2)4-NH2
上式の左端の官能基のアミノ基-NH2がA1とアミド結合し, 右端のアミノ基-NH2がA5とアミド結合する。したがって, 左端のアミノ基を実線で, 右端のアミノ基を点線で囲むことになる。