問1の答
( ア : 13族) ( イ : メンデレーエフ) ( ウ : 体心立方格子) ( エ : 2)
( オ : 8)
●金属結晶…金属の単体は, 金属原子が金属結合で規則的に配列した結晶をしばしば形成する。結晶の最小単位は, 金属単体においては, 次のように, 体心立方格子, 面心立方格子および六方細密構造などが存在する。
○単体の金属結晶は, 主として次の三つの構造がある。結晶の配位数は注目原子を取り巻く最も近い他の原子の数を意味する(索引[化学入試事項](タ)体心立方格子 106-g1, 679-1-s01参照)。
(1)体心立方格子・・・配位数:8, 格子内原子数:2, 格子内原子体積占有率:68%, 例 K, Ba, Ra, V, Nb, Ta, W. 単位格子図を参照すると, 原子数…(1/8)×8 + 1 = 2
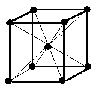 (image1)
(image1)(2)面心立方格子・・・配位数:12, 格子内原子数:4, 格子内原子体積占有率:74%, 例 Al, Pd, Pt, Cu, Ag, Au, Pb. 単位格子図を参照すると, 原子数…(1/8)×8 + (1/2)×6 = 4
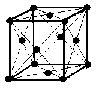 (image2)
(image2)(3)六方最密構造・・・配位数:12, 格子内原子数:6, 格子内原子体積占有率:74%, 例 Mg, Hf, Ru, Os, Zn, Cd. 単位格子図を参照すると, 原子数…(1/6)×12 + (1/2)×2 + 3 = 6
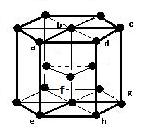 (image6)
(image6)○物質を構成する原子, 分子およびイオンの間の結合は, 主として, 次のように分類される。
化学結合として,
(1)イオン結合…陽イオンと陰イオンとの間に静電的な引力(クーロン力)が働いて結合する。
(例) 塩化ナトリウムNaCl, 硫酸アルミニウムAl2(SO4)3 (Al3+とSO42-がイオン結合), 酸化マグネシウムMgOなど。
(2)共有結合…原子どうしが局在化した電子を共有して結合する…この結合を一般に共有結合という。
(例) 分子中の各原子の結合…メタン分子CH4中の原子CとH, 水分子H2O中の原子HとO, 塩素分子Cl2中の原子Clどうし, ダイヤモンドC中の原子Cどうしなど。
(3)金属結合…多数の陽イオンどうしが多数の非極性の自由電子を共有して結合する。このことは, 金属結合は特異な共有結合を意味する。
(例) 銅Cuや鉄Feなどの金属。
多くの化合物の化学結合は, (1)と(2)の結合をある割合で同時に含む場合が多い…極性分子。
分子の間の結合として,
(1)分子間力による結合
○ 分子間に作用する弱い引力でファンデルワールス力という。一般に, 分子量の大きい分子ほど強い。さらに分子の極性による力が加わる場合がある。
(例) メタンCH4分子, 酸素O2, 塩素Cl2, CO2など。
(2)水素結合
○ 分子中でフッ素原子F, 酸素原子O, 窒素原子Nなどに水素原子Hが結合していると, Hを通して分子間にかなり強い結合を生じる。この結合を特に水素結合という。
(例) 水H2O, フッ化水素HF, アンモニアNH3など。
●単位格子内に含まれるガリウム原子数は, 問題中の図3を参照すると,
(1) 単位格子の直方体の8つの頂点近辺にある原子対数は, 単位格子内に,
(1/8)×8 = 1個
よって, 原子数は,
1×2 = 2個
(2) 単位格子の直方体の上下, 左右および前後の面心近辺にある原子対数は, 単位格子内に,
(1/2)×6 = 3個
よって, 原子数は,
3×2 = 6個
かくして, 単位格子内の全原子数は
(1) + (2) = 2 + 6 = 8個
問2の答 4Ga + 3O2 → 2Ga2O3
ガリウムはアルミニウムと同様に, 原子価は3価であるので, 空気中で加熱すると, 次のように反応して, 酸化物の酸化ガリウム(III) Ga2O3 となる :
4Ga + 3O2 → 2Ga2O3
問3の答 2Ga + 3H2SO4 → Ga2(SO4)3 + 3H2
2Ga + 2NaOH + 6H2O → 2Na[Ga(OH)4] + 3H2
ガリウムはアルミニウム, 亜鉛, スズおよび鉛などと同様に, 両性元素であるので, 希硫酸や水酸化ナトリウム水溶液などの酸・塩基の両方に反応する :
2Ga + 3H2SO4 → Ga2(SO4)3 + 3H2
2Ga + 2NaOH + 6H2O → 2Na[Ga(OH)4] + 3H2
問4の答 42 %
ガリウム原子の 1個の体積は, 球とみなしているので,
(4/3)π(0.250/2)3 ≒0.008177 nm3
単位格子内のガリウム原子の全体積は, 単位格子内に 8個のガリウム原子が存在するので,
0.008177×8 ≒0.06542 nm3
よって, ガリウム結晶の充填率 A は, 単位格子の体積は 0.157 nm3 であるので,
A = (0.06542/0.157)×100 ≒ 42 %
問5の答 水銀
水銀においては, 融点は -38.832℃ および沸点は 356.7℃である。常温で液体(銀白色)の唯一の金属である。
問6の答
結晶内のGa原子対間は距離が長く比較的弱い結合であるので熱運動が小さい低温でも切断して融ける。