問1の答
A…CH3-CH(OH)-CH=CH2, C…CH3-CO-CH2-CH3
ヒント
Aの分子は
(1) 分子式…C4H8O
(2) 1個の不斉炭素原子…1個の炭素原子に全て異なる官能基結合
(3) 臭素付加条件で1個の二重結合存在…-C=C-
(4) ナトリウムと反応して水素ガスが発生…ヒドロキシル基-OH存在
(5) 適切な酸化剤で酸化すると分子式C4H6Oの化合物Dが得られた。Dの分子中には不斉炭素原子はなかった。
(6) Cが1molのDと1molの水素の反応で得られた。Cは分子中には不斉炭素原子はなく臭素とは反応しなかった。
(1)の分子式において(3)を考慮すると構造式中の炭素原子骨格は
-C-C-C=C-, -C-C=C-C-, -C=C(C)-C-
炭素原子骨格に-OHと-Hを結合させると,
CH3-CH2-CH=CH-OH, CH3-CH2-C(OH)=CH2, CH3-CH(OH)-CH=CH2, CH2(OH)-CH2-CH=CH2
CH3-CH=CH-CH2-OH, CH3-CH=C(OH)-CH3
CH2=C(CH3)-CH2-OH, HO-CH=C(CH3)-CH3, CH2=C(CH2OH)-CH3
上の9つの式において(2)と(4)を考慮すると, Aは不斉炭素原子をもつ2級アルコールである(下の式中のC*:不斉炭素原子)。
CH3-C*H(OH)-CH=CH2(答)
CH3-CH(OH)-CH=CH2には, 光学異性体は存在するが, 幾何異性体は存在しない。
(5)によって, Aを適切な酸化剤で酸化すると2級アルコール脱水反応で分子式C4H6Oの化合物D(不斉炭素の無いケトン)が得られるので,
D:CH3-CO-CH=CH2
(6)から, Cは1molのDと1molの水素との付加反応で得られる。
C:CH3-CO-CH2-CH3(答)
Cでは臭素は付加せず, 不斉炭素は存在しないので, 上のCの式は答として妥当である。
問2の答
CH3-O-CH2-CH=CH2, CH3-CH2-O-CH=CH2, CH2=C(CH3)-O-CH3,
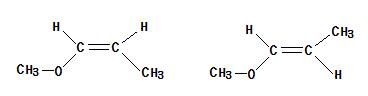 (image189)
(image189)ヒント
Bの分子は
(1)分子式はC4H8Oでエーテル…-O-基存在
(2) 臭素付加より1個の二重結合-C=C-存在
(3) 不斉炭素原子無し
(2)を考慮すると構造式中の炭素骨格は
-C-C-C=C-, -C-C=C-C-, -C=C(C)-C-
上の炭素原子骨格にエーテル基-O-と-Hを結合させると,
CH3-O-CH2-CH=CH2, CH3-CH2-O-CH=CH2
CH3-O-CH=CH-CH3(幾何異性体有),
CH2=C(CH3)-O-CH3,
上の式は不斉炭素原子がないので妥当である。
問3の答
 (image190)
(image190)ヒント
問1の解答ヒントの中で, すでに, Dの構造式は次のように示されている。
CH3-CO-CH=CH2
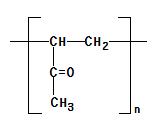
Dの構造式中には, 二重結合が存在するので, 適当な反応条件で, 次のように, Dを単体として付加重合の反応が起こり, 高分子化合物が形成される。
nCH3-CO-CH=CH2 → [-CH(COCH3)CH2-]n
問4の答 A:40%, B:25%, C:35%
ヒント
● 問1と2の解答から, A, B, Cの構造式は
A…CH3-CH(OH)-CH=CH2, B…CH3-O-CH2-CH=CH2(5つの中の1つ), C…CH3-CO-CH2-CH3
● 臭素と付加反応をするのは, 二重結合をもつAとBで, その反応式は
CH3-CH(OH)-CH=CH2 + Br2 → CH3-CH(OH)-CHBr-CH2Br …(1)
CH3-O-CH2-CH=CH2 + Br2 → CH3-O-CH2-CHBr-CH2Br …(2)
Cには二重結合がないので付加反応は生じない。
● Aはナトリウムと反応すると
2CH3-CH(OH)-CH=CH2 + 2Na → 2CH3-CH(ONa)-CH=CH2 + H2 …(3)
● 混合物の質量144gの中にA, B, Cが x mol, y mol, z mol 存在すると, 分子量が72から, 次式が成立する。
72(x + y + z) = 144 … (4)
● 半分の質量では, x/2 mol, y/2mol, z/2mol になる。混合物の二等分の1つに十分な量の臭素を反応させると, (1)と(2)の反応式でAの生成物Px, Bの生成物Pyの物質量は,
Px:CH3-CH(OH)-CHBr-CH2Br … x/2 mol(Aと同物質量)
Py:CH3-O-CH2-CHBr-CH2Br … y/2 mol(Bと同物質量)
また, PxとPyの質量gは, 分子量が4C+8H+O+2Br=232から
(x/2 + y/2)×232 = 116(x + y)
Cは臭素と付加反応しない。その質量gは
(z/2)×72 = 36z
臭素を加えた後の質量は176gなので
116(x + y) + 36z = 176
よって
29(x + y) + 9z = 44 … (5)
● 混合物の二等分のもう1つにナトリウムを反応させると標準状態で4.48 Lの水素が発生した。物質量では4.48/22.4 = 0.2 molになる。一方, (3)の反応式から, 生成物CH3-CH(ONa)-CH=CH2と発生水素H2の物質量比は2:1なので次式が成立する。
x/4 = 0.2
よって,
x = 0.80 mol
(5)式から
29(0.8 + y) + 9z = 44 …(6)
(4)式から
(0.8 + y + z) = 2 …(7)
(7)式を(6)式に代入すると
29(0.8 + y) + 9(2 - 0.8 - y) = 44
20y = 10
よって
y = 0.50 mol
(7)式から z = 0.70 mol
A, B, Cのモル百分率%は
A…0.8/(0.8 + 0.5 + 0.7)×100 = 40 %(答)
B…(0.5/2)×100 = 25 %(答)
C…(0.7/2)×100 = 35 %(答)