[問題] 次の本文について下の各問いに答えなさい。
物質は固体, 液体, 気体の(ア)が存在する。その中で固体は, 固体を構成する粒子間の(イ)や配列などを決める総和エネルギーが熱運動エネルギーよりも大きいときに生じ, その結果として, 粒子の位置が(ウ)。
原子, イオン, または分子などの粒子が空間的周期性を持って規則的に立体的網目構造で配列している固体を特に(エ)という。(エ)の種類は, 構成する粒子の間の結合の種類に注目すると, (オ)…塩化ナトリウムや酸化マグネシウムなど, (カ)…ダイヤモンドや石英など, (キ)…鉄や銅, (ク)…氷やナフタリンなどに分けられる。
(エ)は, 立体的網目構造を意味する空間格子に注目すると, 最小単位の立体の形状と対称性によって7つの型(晶系)に分属する14種の(ケ)に分けられる。
粒子(格子点)の配列の繰り返しを最小単位とする(ケ)には, 一般に(コ)格子が使われる。同金属原子の(キ)は,①(コ)格子の中の面心立方格子, 体心立方格子および六方最密構造の3つから成り立つ。
問1 本文の(ア)~(コ)に最も適した語句を入れなさい。
答
問2 塩化ナトリウム, 酸化マグネシウム, ダイヤモンド, 石英, 鉄, 銅, 氷, ナフタリンの化学式を書きなさい。
答
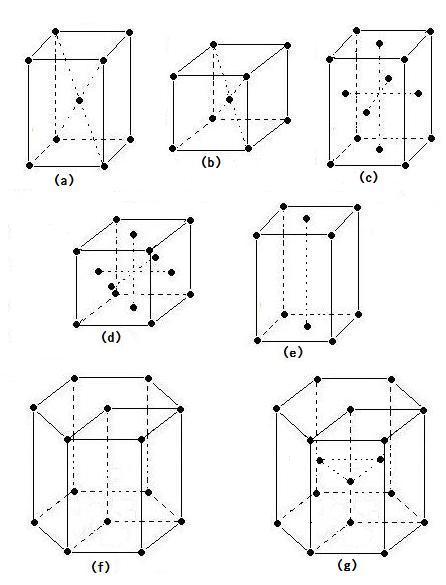
問3 本文の下線部①の面心立方格子, 体心立方格子および六方最密構造は, 下図(a)~(g)のどれに相当しますか。また, 各格子および構造中の原子数と配位数を書きなさい(image181)。
答
問4 次の文を読み下の問い(1)~(3)に答えなさい。ただし, ( )のカタ仮名は本文のものと一致する。答の有効数字は三桁とする。
必要あれば次の数値を利用してもよい。(2)1/2 = 1.414, (3)1/2 = 1.732
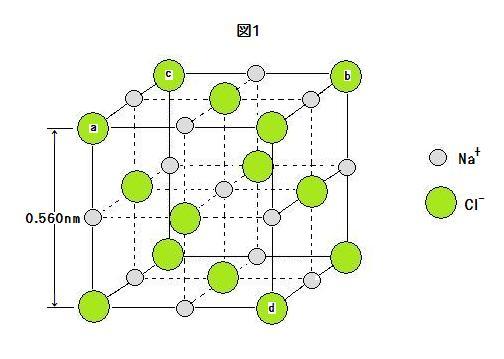
(オ)は多数の陰陽のイオンがイオン結合をして形成された(エ)である。塩化ナトリウム(エ)はイオン式で表わすとNa+Cl-となり, 図1(image182)の実線で示した立方体の(ケ)からなる。図1の(ケ)中ではCl-が面心立方格子をつくりその間にNa+が存在している。酸化マグネシウム(エ)も(オ)でイオン式は(A)で表わされる。塩化ナトリウム(エ)において, Na+とCl-のイオンは(ケ)あたりともに正味(B)個ずつ存在する。したがって, 1nm3の体積中には, Na+とCl-のイオン数はともに(C)個である。図1中の3点abcとabdを通る2つの平面を考え, このような平面を格子面と呼ぶことにする。平面abc内に中心を持つNa+とCl-の, 平面abc 1nm2あたりのイオン数はそれぞれ(D)個と(E)個である。同様にして, 平面abdにおいてはそれぞれ(F)個と(G)個である。
(オ)は, 一般に機械的強度は小さく衝撃を与えると一定方向に割れやすい。これは, 衝撃が加わるとイオンの位置が格子面に沿ってずれ, その面を境に(オ)が割れることを意味する。塩化ナトリウム(エ)では, ②平面abdに平行な格子面に沿ってよりも平面abcに平行な格子面に沿って割れやすい。
(1) 上の文の(A)に適切なイオン式を書きなさい。
答
(2) 上の文の(B)~(G)に適切な数値を記入しなさい。
答
(3) 上の文の下線部②の理由を150字以内で説明しなさい。
答