Japanese-English Exam Similar Question 5-2
酸化カルシウム形成に対するBorn-Haber サイクルが下に示されている :
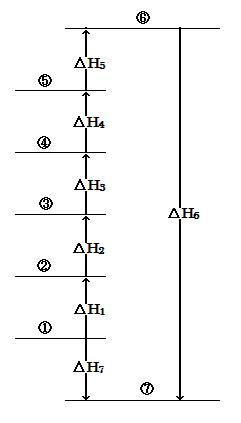
各エネルギーレベル状態 :
①;Ca(s) + (1/2)O2(g) ②;Ca(g) + (1/2)O2(g) ③;Ca(g)+ + (1/2)O2(g) + e-
④;Ca(g)2+ + (1/2)O2(g) + 2e- ⑤;Ca(g)2+ + O(g) + 2e- ⑥;Ca(g)2+ + O(g)2- ⑦:CaO.
各標準エンタルピー変化 ΔH/kJ mol-1 :
ΔH1 = +193; ΔH2 = +590; ΔH3 = +1150; ΔH4 = +248; ΔH6 = -3513; ΔH7 = -635.
下の問1と問2に答えなさい。
問1
(i) ΔH2 の値は何のエンタルピー変化を表わしていますか ?
答
(ii) ΔH2 の値はカルシウムよりもマグネシウムの方が大きいですか, それとも小さいですか ?
答
(iii) 問1(ii)においての答を説明しなさい。
答
A Born-Haber cycle for the formation of calcium oxide is shown below :
 (image522)
(image522) Each of energy level states :
①;Ca(s) + (1/2)O2(g) ②;Ca(g) + (1/2)O2(g) ③;Ca(g)+ + (1/2)O2(g) + e-
④;Ca(g)2+ + (1/2)O2(g) + 2e- ⑤;Ca(g)2+ + O(g) + 2e- ⑥;Ca(g)2+ + O(g)2- ⑦:CaO.
Each of standard enthalpy change data ΔH/kJ mol-1 :
ΔH1 = +193; ΔH2 = +590; ΔH3 = +1150; ΔH4 = +248; ΔH6 = -3513; ΔH7 = -635.
Answer the questions below, Q1and Q2.
Q1
(i) What enthalpy change does the value of ΔH2 represent ?
Answer
(ii) Would the value of ΔH2 be larger or smaller for magnesium than it is for calcium ?
Answer
(iii) Explain your answer in Q1(ii).
Answer
問2 炭酸カルシウムでの不純物である固体の塩化カルシウムを取り上げて, カルシウムイオンと塩化物イオンの存在を確認するために試行するテストを記述しなさい。
(i) カルシウムイオン :
答
(ii) 塩化物イオン :
答
Q2 Given a sample of solid calcium chloride, contaminated with calcium carbonate, describe tests you would perform in order to confirm the presence of :
(i) calcium ions :
Answer
(ii) chloride ions :
Answer